空氣和氧氣
一、空氣的組成
1.空氣的成分和組成
(1)氮氣
通常狀況下,氮氣是無色、無味的氣體,難于水。常溫下化學性質穩定。氮氣不支持燃燒也不供給呼吸。它是制造硝酸和化肥的 重要原料;根據氮氣常溫下化學性質穩定,氮氣可用作保護氣,如焊接金屬時常用氮氣作保護氣,食品包裝時充氮氣以防腐;醫療上 可用液氮作冷凍劑等。
(2)稀有氣體
氦氣、氖氣、氬氣、氪氣、氙氣、氡氣等氣體在空氣中含量少且化學性質穩定,化學上把它們總稱為稀有氣體,又稱惰性氣體。稀有氣體通常可用作保護氣;稀有氣體通電時會發出各種顏色的光,可用作霓虹燈等。
(3)臭氧(O3)
是大氣中一種很重要的氣體,它的重要性質是抵御紫外線,保護地球上的生物免受緊外線傷害。
2.空氣中氧氣含量的測定
(1) 實驗原理:利用磷燃燒消耗空氣中的氧氣,從而使容器內形成負壓,打開止水夾后,水進入容器內。進入容器中的水的體積,可 粗略地認為是空氣中所含氧氣的體積。
(2)實驗步驟及現象:
①在集氣瓶中放入少量水(用于溶解生成的五氧化二磷,同時可吸收燃燒產生的熱,有利于瓶內降 溫),做上記號,并將瓶內剩余體積均分為五等分。
②用止水夾夾緊乳膠管,點燃燃燒匙內的紅磷后,立即伸入集氣瓶中并把塞子塞緊。觀察到紅磷燃 燒,產生濃厚的白煙。
③紅磷熄滅后,冷卻至室溫,打開止不夾,觀察到水進入集氣瓶內,最終水面在五分之一記號處。
(3)實驗結論:
①空氣是混合物;
②O2約占 1/5,可支持燃燒;
③其它氣體約占 4/5,不支持燃燒,也不能燃燒,難溶于水
(4)實驗反思與改進:
①反應物選擇及用量:
選擇過量的紅磷是為了將氧氣完全轉化為固體物質,形成壓強差,水倒流占據氧氣體積,便于觀察。
如果選擇碳或者硫,則會形成氣態物質,無法形成壓強差,需在右側燒杯中使用氫氧化鈉溶液,可以吸收產物二氧化碳和二氧化 碳,同樣可以形成壓強差,實驗也可以成功;
如果選擇鐵絲,則由于不能在空氣中燃燒而無法消耗氧氣,實驗無法成功;
鎂條呢?然而,由于鎂會與氧氣、氮氣、二氧化碳均發生反應,則最終水倒流占據了三者體積和,顯然遠大于五分之一,實驗無 法成功。
②氣密性:
該實驗涉及氣體體積測量,需在實驗開始前進行氣密性檢查,在實驗過程中也需保持氣密性良好,紅磷需先引燃后放入集氣瓶, 插入燃燒匙時,瓶口的氣體已經受熱膨脹,造成氣體逸出,壓強差會增大,最終測量結果會偏大。如何改善實驗過程呢?
如下圖所示,用著火點較低的白磷代替紅磷,用聚光、熱傳遞等方式引燃白磷,確保實驗過程的氣密性良好。
③溫度:
溫度升高,則氣體受熱膨脹,壓強增大,則瓶內壓強與大氣壓強差值 變小,水流入量偏小,為避免溫度對實驗的影響,需冷卻到室溫后打開止水夾。
3.空氣的污染及防治:
(1)明確空氣質量三大指標:可吸入顆粒物(包含 PM2.5)、二氧化硫、氮氧化合物。只要是有毒氣體,均為大氣污染氣體,如 CO、H2S 等
二氧化硫會造成酸雨,其主要來源是工業上大量燃燒含硫燃料,如煤炭燃燒。
(2)防治:為了使天更藍,人類正在積極行動,如加強大氣質量監測,改善環境狀況;使用清潔能源,改善環境狀況;積極植樹、造林、種 草等,以保護環境。
(3)目前環境污染問題:
臭氧層破壞
溫室效應(CO2等)
酸雨(SO2等)
二、氧氣的性質
1.氧氣的物理性質
常溫下,氧氣是無色無味的氣體,難溶于水,密度比空氣略大。
2.氧氣
(1)氧氣的化學性質:
支持燃燒,供給呼吸。檢驗氧氣:用帶火星的木條伸入瓶內,復燃則是氧氣。
(2)氧氣與很多物質反應現象
注意:
①鐵燃燒實驗:
需將鐵絲繞成螺旋狀的目的:增大與空氣接觸面積,使反應容易發生。
燃燒時需用火柴引燃:提高溫度,使其達到鐵的著火點。火柴幾乎熄滅時插入集氣瓶內:防止火柴消耗過多氧氣,影響鐵絲的燃燒。
要在集氣瓶底部放少量水或細砂的目的:防止濺落的高溫熔化物 Fe3O4炸裂瓶底。
鐵在空氣中不可燃燒:氧氣濃度越高,可燃物燃燒程度越劇烈。
②硫燃燒實驗:
要在集氣瓶底部放少量水:吸收二氧化硫,防止污染空氣。
碳及其化合物
一、碳的單質
1.碳的同素異形體
說明:無定形碳是混合物,不是碳同素異形體,如木炭、焦炭、活性炭(吸附性)、炭黑。
2.碳的化學性質
化學是一門研究物質的組成、結構、性質以及變化規律的自然科學。
二、碳的氧化物
1.一氧化碳與二氧化碳
2.一氧化碳與碳還原氧化銅的比較
3.碳及其氧化物的轉化關系
三、家用燃料
1.燃燒的定義
具有劇烈的發光發熱現象的化學反應,稱作可燃物的燃燒。
2.燃燒的條件
(1)存在可燃物
(2)可燃物接觸助燃劑:最常見的就是空氣中的氧氣。二氧化碳氣體也可作為某活潑金屬(例如鈉、鎂)的助燃劑,如:
現象:劇烈燃燒,發出白光,生成白色粉末和黑色固體)。
(3)溫度達到著火點:著火點指可燃物著火燃燒所需的最低溫度。
注意:三個條件同時滿足才能發生燃燒現象,缺一不可。
3.滅火的原理
消除可燃物或使可燃物與其他物品隔離,隔絕氧氣(或空氣),以及使溫度降到著火點以下,都能達到滅火的目的。
4.燃料的充分燃燒
不間斷地鼓入足量的空氣(氧氣);
增大接觸面積,把固體燃料進行粉碎,把液體燃料噴成霧狀;
有效改進設備,防止反應熱量的散失。
5.常見的家用燃料
天然氣:主要成分是甲烷,是一種氣體化石燃料。甲烷是一種無色無味的氣體,極難溶于水,密度比空氣小,所以實驗室可以用 排水法或向下排空氣法收集。甲烷是一種可燃性氣體,點燃前必須先驗純,純凈的甲烷在空氣中安靜燃燒,火焰呈淺藍色,生成二氧 化碳和水。燃燒產物無污染,所以天然氣是一種清潔(或綠色)能源。
氫能是最理想的綠色能源,理由是來源廣泛,燃燒生成水,無污染,燃燒產生的熱量多等。
酸堿鹽
一、酸
1.酸的組成
酸是僅由氫元素和酸根組成的化合物。
【注意】以下物質不是酸:NaHCO3、H2O
2.酸的分類
①有機酸和無機酸:
常見的無機酸:HCl、HNO3、H2SO4、H2CO3
常見的有機酸:CH3COOH(乙酸)、HCOOH(甲酸)
②無機酸按酸分子中氫原子個數不同,分為:一元酸、二元酸、三元酸。
如:HCl HNO3為一元酸 ;H2SO4 H2CO3為二元酸;H3PO4為三元酸。
有機酸按照 COOH 的個數不同,分為一元酸、二元酸
如:CH3COOH 為一元酸
③按是否含有氧分為:
含氧酸和無氧酸 含氧酸的命名規則為“某酸”:例如 H2CO3命名為碳酸
無氧酸的命名規則為“氫某酸”:例如 H2S 命名為氫硫酸
3.酸的通性:
酸的組成中均含有氫,因此酸具有相似的性質。
①酸溶液與指示劑反應。
②酸 + 活潑金屬(活動性順序表中排在 H 前的金屬) → 鹽 + H2↑
鐵釘和鹽酸反應:Fe+2HCl →FeCl2+H2↑ 現象:鐵釘溶解,有氣泡產生,溶液逐漸變為淺綠色。
【注意】一般采用稀硫酸或者稀鹽酸,濃鹽酸揮發性太強,產生的氫氣中含有大量氯化氫氣體,濃硫酸或硝酸與金屬反應不產生氫氣。
③酸與某些鹽反應:
(1)與碳酸鹽、碳酸氫鹽反應生成二氧化碳:
實驗室制取二氧化碳:CaCO3+2HCl → CaCl2+H2O+CO2↑實驗現象:有氣泡產生
小蘇打可以緩解胃酸過多:NaHCO3+HCl→NaCl+H2O+CO2↑
(2)與一些鹽反應生成沉淀:
用氯化鋇溶液檢驗硫酸:BaCl2+H2SO4→ BaSO4↓+2HCl 實驗現象是:有白色沉淀產生
用硝酸銀溶液檢驗鹽酸:AgNO3+HCl → HNO3+AgCl↓ 實驗現象是:有白色沉淀產生
④ 中和反應:酸 + 堿 → 鹽 + 水
(1)定義:酸和堿反應,生成鹽和水并放出熱量的反應稱為中和反應。
如:3HCl + Fe(OH)3 → FeCl3 + 3H2O實驗現象是:紅褐色沉淀逐漸溶解,溶液變為棕黃色。
H2SO4 + 2NaOH → Na2SO4 + 2H2O無法觀察到明顯現象。
(2)中和過程中溫度和 pH 變化
以將稀硫酸注入氫氧化鈉溶液為例:
(3)中和反應的應用:
Ca(OH)2:改良酸性土壤。
Mg(OH)2、Al (OH)3:治療胃酸過多。
⑤ 酸 + 金屬氧化物 → 鹽 + 水
堿性氧化物定義:像氧化鐵、氧化銅,能跟酸反應生成鹽和水的氧化物叫做堿性氧化物。大多數金屬氧化物是堿性氧化物。
稀鹽酸或稀硫酸除鐵銹:
Fe2O3 + 6HCl → 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
實驗現象:銹逐漸減少,溶液由無色變成黃色
黑色的氧化銅跟稀鹽酸或稀硫酸反應:
CuO + 2HCl → CuCl2 + H2O
CuO + H2SO4 → CuSO4 + H2O
實驗現象是:黑色的固體逐漸溶解,溶液由無色變成藍色。
4.常見的酸
①鹽酸
(1)鹽酸的物理性質:
鹽酸是無色透明的液體,有刺激性氣味,具有揮發性。
【注意】純凈的鹽酸為無色液體,工業鹽酸因含FeCl3而顯黃色。
(2)揮發性:
鹽酸濃度越大,揮發性越強。濃鹽酸瓶口出現白霧,這是由于揮發出來的氯化氫氣體與空氣中的水蒸氣接觸,又形成鹽酸小液滴 的緣故。
鹽酸具有揮發性,所以實驗室必須密封保存,敞口放在空氣中,溶質質量減小,溶液濃度會變小。
②硫酸
(1)物理性質:
純凈的硫酸是無色、粘稠、油狀的液體,不 易揮發,易溶于水并放出大量的熱。
濃硫酸稀釋時,需把濃 H2SO4沿容器壁慢慢注入水中且邊倒邊攪拌,切不可將水倒入濃硫酸。
皮膚上沾上濃硫酸,先用棉布吸去酸,后用清水沖洗,再用 3%~5%的小蘇打溶液沖洗
(2)吸水性:
濃硫酸吸收空氣中的水蒸氣,使溶質的質量分數減小,沒有生成新物質,是物理變化。由于濃硫酸具有吸水性,所以實驗室必須 密封保存。
利用濃硫酸具有吸水性,在實驗室可以用作干燥劑,除堿性的氨氣不可以,幾乎可以干燥所有的氣體。
(3)脫水性:
原物質中沒有水,將原物質中的氫、氧兩種元素按水的組成比(2:1)脫去,是化學變化。
濃硫酸點到 pH 試紙上,試紙變成黑色,因此無法用 pH 試紙檢測濃硫酸酸堿度。
二、常見的堿
1.堿的組成:
堿是僅由金屬元素(或銨根)和氫氧根組成的化合物。
2.堿的分類
按照溶解性:
可溶性堿:NaOH,KOH,Ba(OH)2,Ca(OH)2,NH3·H2O
難溶性堿:其余的堿,如:Cu(OH)2、Fe(OH)3
按照堿性強弱:
強堿:NaOH,KOH,Ba(OH)2,Ca(OH)2
弱堿:其余的堿,如 NH3·H2O
3.堿的通性
① 堿溶液能使指示劑變色:
堿溶液使紫色石蕊溶液變藍,使無色酚酞溶液變紅。
② 與非金屬氧化物反應生成鹽和水
酸性氧化物:像二氧化碳、二氧化硫等能跟堿溶液反應生成鹽和水的氧化物叫做酸性氧化物。非金屬氧化物大多是酸性氧化物。
2NaOH + CO2 → Na2CO3 + H2O (NaOH 應密封保存)
2NaOH + SO2 → Na2SO3 + H2O
③ 與酸發生中和反應
2NaOH + H2SO4 → Na2SO4 + 2H2O
④ 與某些鹽反應
FeCl3 + 3NaOH → Fe(OH)3↓+ 3NaCl(NaOH 常用于制不溶性堿)
4.常見的堿
① 氫氧化鈉與氫氧化鈣
②Cu(OH)2:藍色粉末固體,難溶于水。
③Fe(OH)3:紅褐色同體,難溶于水。
三、鹽
1.鹽的組成:
鹽是由金屬元素(或銨根)和酸根組成的化合物。
2.鹽的分類和命名:
① 分類
正鹽:只由金屬元素(或銨根)和酸根組成的鹽。
如:NaCl、K2SO4
酸式鹽:金屬元素(或銨根)和酸式酸根組成的鹽。
如:NaHCO3、KHSO4、NaHS
復鹽,如:KAl(SO4)2
,讀作“硫酸鋁鉀”。
② 命名
含有相同的酸根:某酸鹽。
如含硫酸根的鹽(CuSO4、K2SO4、CaSO4等)統稱為“硫酸鹽”
含有相同的金屬元素:某鹽。如含K元素的鹽(KCl、K2SO4、K2CO3等)統稱為“鉀鹽”
3.鹽的溶解性
溶解性口訣:
鉀鈉銨硝四鹽皆可溶;
硫酸鹽中鋇不溶;(硫酸鈣,硫酸銀微溶)
鹽酸鹽中銀不溶;
碳酸鹽只溶鉀鈉銨。
其中硫酸鋇、氯化銀超級難溶,既不溶于水也不溶于酸
【記憶技巧】
常見八個沉淀:
4. 鹽溶液的顏色
無色——多數
藍色:銅鹽溶液——CuCl2、CuSO4、Cu(NO3)2
淺綠色:亞鐵鹽溶液——FeCl2、FeSO4、Fe(NO3)2
黃色:鐵鹽溶液——FeCl3、Fe2(SO4)3、Fe(NO3)3
5. 鹽的通性
① 金屬+鹽溶液→新金屬+新鹽
條件:前換后(K、Ca、Na除外)、鹽必溶;混合鹽溶液中,間隔大先進行
金屬活動性順序:
K Ca Na Mg Al Zn Fe Sn Pb (H) Cu Hg Ag Pt Au
② 酸+某些鹽→酸+鹽
條件:生成氣體或者沉淀
HCl+AgNO3→HNO3+AgCl↓(檢驗鹽酸鹽)
H2SO4+BaCl2→2HCl+Ba2SO4↓檢驗硫酸鹽)
2HCl +CaCO3→CaCl2+H2O+CO2↑(實驗室制CO2)
③ 堿+鹽→新堿+新鹽
條件:可溶性堿和可溶性鹽生成難溶性物質或弱堿
Ca(OH)2+Na2CO3→CaCO3↓+2NaOH
2NaOH+CuSO4→Na2SO4+ Cu(OH)2↓
④ 鹽+鹽→新鹽+新鹽
條件:兩種可溶性鹽生成一種或兩種難溶性鹽
2AgNO3+BaCl2→Ba(NO3)2+2AgCl↓
Na2CO3+CaCl2→2NaCl+CaCO3↓
四、金屬
1.金屬的物理性質
2.金屬的化學性質
(1)金屬與酸的置換反應
在金屬活動性順序里,只有排在氫前面的金屬才能置換出酸中的氫。
如:Zn+ H2SO4(稀)→ZnSO4+H2↑,Mg + 2HCl → MgCl2 + H2↑
(2)金屬與鹽溶液的置換反應
在金屬活動性順序里,排在前面的金屬(K、Ca、Na 除外)能把排在后面的金屬從其鹽溶液中置換出來,且鹽必須溶于水,否則不反應。
【注意】
①活潑金屬與酸反應時,酸一般指的是稀鹽酸或稀硫酸,當金屬與濃硫酸或硝酸反應時,不產生 H2。
②用金屬跟鹽溶液發生反應時,一般不用很活潑的 K、Ca、Na 等,因為這些金屬常溫下和水發生反應,而不能置換出鹽溶液里的金屬。
③Fe 參加與酸或鹽溶液的置換反應時,生成物中鐵元素為+2 價,不可寫成+3 價鐵的化合物。
④設計實驗驗證金屬活動性順序時,如果從與酸反應的劇烈程度來判斷,則要按控制變量的方式保證金屬大小與薄厚相同,表面氧化 膜都要用砂紙打掉,且所選擇的酸的濃度、體積、溫度都一樣。如果從前置換后的角度來比較,可選擇依次置換的方式來進行。
3.金屬的冶煉
一氧化碳煉鐵的原理:
實驗室中一氧化碳與氧化鐵反應的裝置:
實驗中產生的現象主要有哪三點:紅棕色的氧化鐵粉末逐漸變成黑色,同時澄清的石灰水逐漸變渾濁,尾氣燃 燒并產生淡藍色火焰。
4.金屬活動性強弱
在金屬活動性順序中,排在氫前面的金屬能置換出稀鹽酸或稀硫酸中的氫,排在氫后面的金屬不能置換出稀鹽酸或稀硫酸中的氫。只有排在前面的金屬,才能把排在后面的金屬從它們的鹽溶液中置換出來。
【注意】金屬活動性順序可采用“五元素一句”的方法記憶,即“鉀鈣鈉鎂鋁,鋅鐵錫鉛(氫),銅汞銀鉑金”。
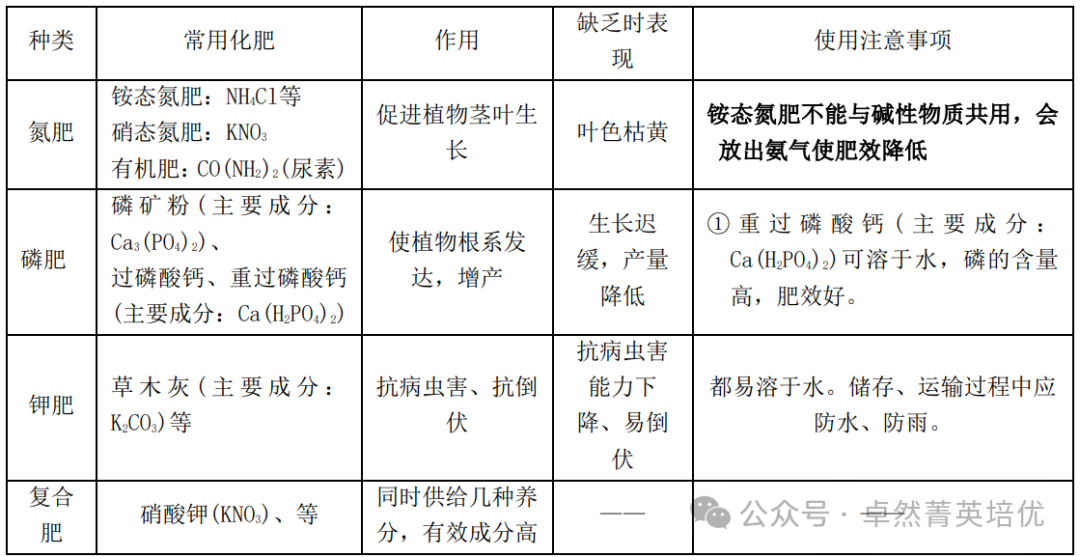
五、化肥